
四川大学华西医院肾脏内科苏白海教授团队于2020年5月在Carbohydrate polymers(影响因子7.182,在JCR“有机化学”类别57种期刊中排名第2位)在线发表文章"Anticoagulant chitosan-kappa-carrageenan composite hydrogel sorbent for simultaneous endotoxin and bacteria cleansing in septic blood"(长按下方二维码即可阅读全文)
|
脓毒症指继发于感染、威胁生命的器官功能衰竭,它是重症监护病房中引起患者急性肾损伤的最主要原因,其在全球范围内的年发病人数超过3150万,导致530万人死亡。目前,脓毒症的治疗主要包括广谱抗生素抗感染治疗、液体复苏及必要时血管升压药治疗等;但在这些传统治疗下,脓毒症患者的死亡率仍高达20%,重症脓毒症和脓毒性休克患者的死亡率则更高。血液净化治疗是重症脓毒症和脓毒性休克患者重要的辅助治疗。在脓毒症中,血液中较高的内毒素(脂多糖)浓度和细菌负荷均与患者多器官功能衰竭严重程度及病死率密切相关。然而,临床现有的用于脓毒症患者内毒素吸附的血液净化设备(如Oxiris膜及多黏菌素B吸附柱等)均由国外公司生产,技术垄断问题日益突出,且这些技术在治疗过程中无法同时清除脓毒症患者体内的内毒素及细菌,严重影响治疗效果。本研究的主要目的是提供一种制备自抗凝的、具有内毒素吸附功能的国产血液灌流器的方法,并通过体外实验验证其临床应用的可行性。
壳聚糖(chitosan)是自然界中的一种天然多糖,来源广泛,生物相容性好。前期研究表明壳聚糖与内毒素之间有较高的亲和力,可在蛋白质溶液吸附内毒素,实现内毒素的分离。同时,壳聚糖具有一定的抑菌功能,在血液中应用时可非特异性地减少脓毒症患者血液中的致病细菌负荷(包括革兰阳性及阴性菌)。因而,本研究选择壳聚糖作为制备内毒素吸附剂的载体和配体,简化了传统血液灌流吸附剂制备过程中利用不同化学接枝方法将配体固定在载体表面的复杂过程。如图1所示,我们首先利用相转化法制备了壳聚糖微球(Chitosan hydrogel);然后进一步通过京尼平(genipin)交联得到交联壳聚糖微球(C2 hydrogel),提升吸附剂的机械强度以满足血液灌流治疗对吸附剂力学性能的需要;最后在吸附剂的表面引入具有抗凝活性的卡拉胶(kappa-carrageenan)凝胶层,合成最终的壳聚糖/卡拉胶杂合微球(C-K hydrogel),即目标自抗凝血液灌流吸附剂(下文简称吸附剂),以提升吸附剂的血液相容性。随后,我们对该吸附剂进行了系统的化学结构表征(红外光谱分析、X射线光电子能谱及热失重分析等,结果见已发表论文,DOI: 10.1016/j.carbpol.2020.116470),结果表明该吸附剂已被成功制备。
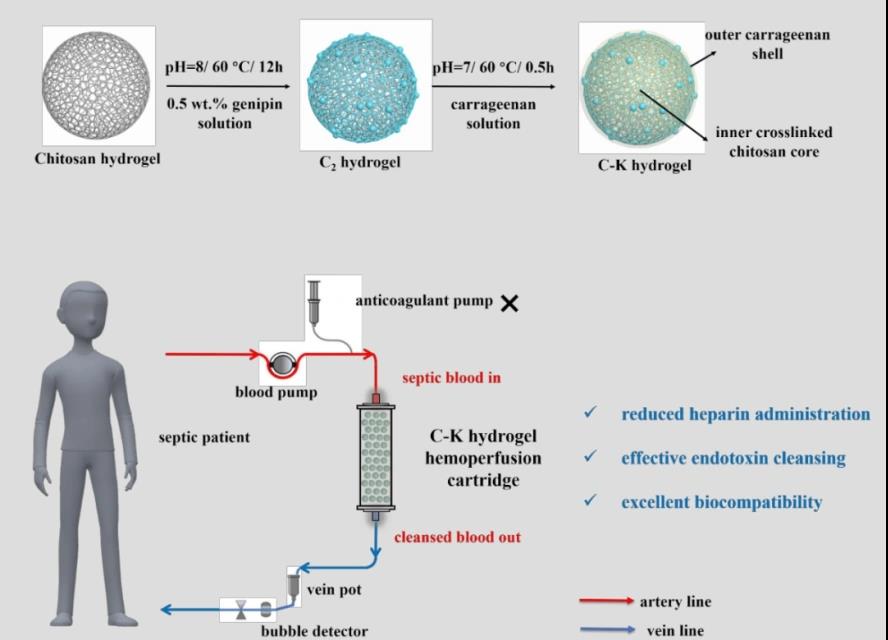
图1 自抗凝血液灌流吸附剂的制备方法及其应用示意图
图2 展示了扫描电镜下该吸附剂表面的典型超微结构。在引入卡拉胶后,微球表面出现了一层粗糙的卡拉胶凝胶层,作为接触血液的主要界面,发挥抗凝作用。这种核壳结构的材料设计虽然一定程度上降低了吸附剂的孔隙率,降低了吸附剂对内毒素的理论吸附值,但同时也提升了吸附剂的血液相容性(吸附剂表面蛋白吸附下降、凝血系统及补体激活减少,结果见已发表论文,DOI: 10.1016/j.carbpol.2020.116470),保证了该吸附剂在重症脓毒症患者血液净化中的安全应用。

图2 自抗凝血液灌流吸附剂表面的典型扫描电镜照片
脓毒症患者体内存在着明显的凝血系统激活,极易导致弥散性血管内凝血(disseminated intravascular coagulation, DIC)等并发症的发生。DIC反过来又造成血液系统中血小板及凝血因子的丢失,增加了脓毒症患者在接受血液净化时的出血风险,传统的抗凝治疗在应用时可能因此受限。本课题组前期两项重要成果表明带有抗凝功能的新型血液接触材料(血液灌流器、血液透析器)可显著地降低患者在接收血液净化时的出血风险,更好地保护具有高出血风险的重症脓毒症患者(Zhao WF, Liu Q, Zhang X, et al. Rationally designed magnetic nanoparticles as anticoagulants for blood purification. Colloids Surf B Biointerfaces, 2018, 164: 316-323;Song X, Ji HF, Li YP, et al. Pseudo-haemophilia blood-thinning strategy for safe extracorporeal blood purification. Nat Biomed Eng. In press)。因此,本研究着重讨论了该吸附剂的抗凝性能及抗凝机制。如图3a所示,该吸附剂可显著地延长血浆活化部分凝血活酶时间(activated partial thromboplastin time, APTT)及凝血酶原时间(thrombin time, TT),吸附剂的抗凝效果与表面卡拉胶的含量正相关;作为一种优选的配方,C2-K1 微球可将血浆APTT及TT分别延长到110s和37s;该吸附剂的抗凝性能与卡拉胶可明显降低血浆中内源性凝血因子(Ⅷ、Ⅸ、Ⅺ和Ⅻ)活性这一作用相关(图3c),而与血浆中抗凝血酶Ⅲ活性无关(图3d)。图3b则提示该吸附剂与血浆接触后纤维蛋白原的浓度仍可保持在正常范围。因而,我们认为该吸附剂在未来应用时有望减少甚至避免传统抗凝剂在脓毒症患者血液净化中的使用,降低出血风险,更好地保护患者。

图3 自抗凝血液灌流吸附剂的抗凝性能及机制
*,与Blank control比较,P<0.05;#,与C2比较,P<0.05;ns,与Blank control比较,P>0.05
我们在体外构建了该吸附剂对内毒素的静态及动态吸附模型(图4a),按图4f的血液灌流示意流程,通过测定吸附前后血液/磷酸盐缓冲液(phosphate-buffered saline, PBS)中内毒素浓度的变化计算出吸附剂对内毒素的清除率及吸附量,系统地研究了卡拉胶含量、内毒素初始浓度、吸附时间等因素对吸附剂内毒素清除效果的影响。作为一种优选的配方,C2-K1 微球在PBS中内毒素的静态吸附量达到202.8 EU/g(图4b),在全血中对内毒素的吸附量达到95.0 EU/g,清除率为63.3%(图4e);吸附在3 h逐步达到饱和,与临床血液灌流治疗时间契合。与临床现有的Oxiris膜及多黏菌素B吸附柱,以及其他研究所提出的内毒素吸附剂相比,我们所制备的自抗凝血液灌流吸附剂的内毒素清除效果更佳(图4e),且独具抗凝功能,具有一定的优势。
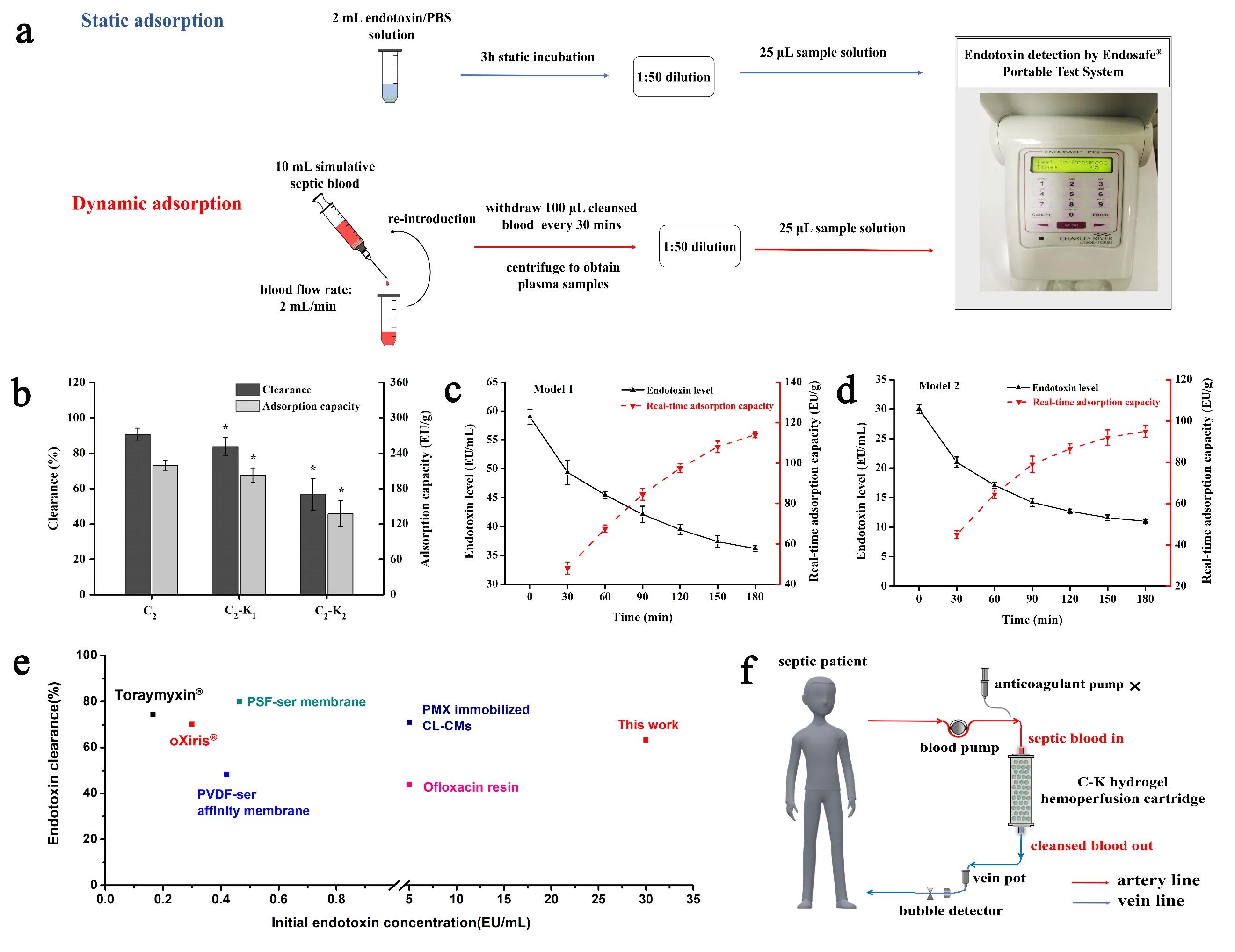
图4 自抗凝血液灌流吸附剂的内毒素吸附性能
*与C2比较,P<0.05
此外,脓毒症患者治疗时需要通过耗时的血培养结果来明确致病菌;这导致部分患者因不匹配的抗生素治疗而出现治疗效果不佳、抗生素不良反应等问题,严重影响脓毒症患者预后。既往已有多项研究报道了壳聚糖对革兰阳性及阴性菌的抑菌功能,在本研究中我们对吸附剂的抑菌性能进行了初步的研究,我们的结果与既往研究一致。该吸附剂可非选择性降低血液中金黄色葡萄球菌(S. aureus,68.7%)及大肠杆菌(E. coli,48.0%)的细菌负荷。结果见图5。这种非特异性的抑菌性能在脓毒症早期可以与广谱抗生素协同作用,更好地控制住脓毒症患者体内的感染情况,为今后脓毒症的治疗提供一种新思路。

图5 自抗凝血液灌流吸附剂的非特异性抑菌性能
*,与Control比较,P<0.05;ns,与C2比较,P>0.05
综上所述,我们提出了一种制备自抗凝的、具有内毒素吸附功能的血液灌流吸附剂的新方法,并在体外验证了其应用于临床的可行性。该方法已申请国家发明专利2项并获得授权(专利号:ZL 2019 1 0758030.1);该吸附剂的后续转化将在四川大学华西医院科技成果转化基金“自抗凝壳聚糖杂合血液灌流吸附柱用于脓毒血症患者体外内毒素吸附及细菌捕获的转化研究(项目编号:CGZH19006)”资助下继续有序进行。我们希望能够通过后续的努力逐步推动该项目的成功转化,突破国外技术垄断,早日研发出中国第一款国产内毒素血液灌流吸附器,造福于患者。

Carbohydrate Polymers为有机化学、应用化学、高分子科学领域的顶级期刊(JCR分别排名2/57、3/71和4/89),杂志对投稿论文格式及内容创新性均有很高要求。本论文选题来源于临床实际,旨在提供可实现脓毒症患者血液中内毒素吸附的国产血液灌流器的制备方法,突破国外技术封锁,具有重大的社会经济价值。同时,在课题组前期对抗凝血液接触材料研究的基础上,本研究进一步地从机理上探索生物材料的抗凝机制,增加了研究结果的说服力;论文全文共16 000字,通过25张图表系统地阐述了该内毒素吸附剂的制备方法、化学结构、血液相容性及毒素清除能力,充分验证了该吸附剂在临床应用的可行性,从而提高了论文质量。在论文修改过程中,我们也针对审稿人提出的问题重新查阅文献并设计实验,通过数据打消审稿人的困惑,使得论文在初次修回后直接接收。
本文的通讯作者为四川大学华西医院肾脏内科苏白海教授,共同通讯作者为四川大学高分子科学与工程学院赵长生教授。四川大学急诊医学博士李育霈、肾脏内科博士李佳梦为本文的共同第一作者。四川大学高分子科学与工程学院赵伟锋副研究员参与了本研究的实验设计、数据分析及论文修改。

苏白海,主任医师、教授、博士生导师,四川大学华西医院肾脏内科副主任/四川大学党委书记。中国生物材料学会血液净化材料分会副主任委员、中国研究型医院肾脏病专委会全国委员、中国医院管理协会血液净化专委会全国青年委员、四川省医学会肾脏病专委会常务委员、四川省学术带头人后备人选、四川省卫生计生委学术技术带头人、中国职工保险互助会医疗鉴定专家、国际肾脏病协会会员、四川省医师协会高血压专委会委员。长期担任临床医学导论教学工作,注重对学生医学人文和从医兴趣的培养,利用自身成长经历、医工结合实践引导医学生树立科技创新、产业报国梦想;目前主要从事血液净化生物材料研发及转化、血液透析并发症、慢性肾脏病及急性肾损伤的诊断和治疗等方面的研究;负责国家十三五重点研发计划“佩戴式人工肾关键技术研发”、国家自然科学基金、四川省科技攻关项目等国家省部级课题8项,累计到校经费600多万;参编著作6部;以第一作者或通讯作者在国内外杂志发表论文50多篇,其中被SCI收录文章30篇;以第一发明人申请国家专利4项;获四川省科技进步二等奖1项;指导学生获得包括2017年全国“互联网+”创新创业比赛金奖及2019年四川省“互联网+”创新创业比赛银奖在内的竞赛奖项共7项,并获得“四川大学青年骨干教师”、“学生心目中最喜爱教师”等多项荣誉。
Email:imsbh@163.com

赵长生,教授,博士生导师,四川大学化学工程学院院长。担任国务院第七届学科评议组成员、中国生物材料学会血液净化材料分会主任委员、中国工程教育认证协会材料类专委会委员、教育部高分子材料与工程专业教指委委员、国家级实验教学示范中心联席会材料学科组组长、中国生物材料学会青年委员会常务理事、中国生物医学工程学会生物材料分会理事、四川省生物医学工程学会常务理事、《中华现代内科学杂志》常务编委、Journal of Membrane and Separation Technology、Journal of Research Updates in Polymer Science 及 International Journal of Polymer Science 编委;长期从事功能高分子研究,特别是聚醚砜血液净化膜、智能和特异分离吸附材料;近五年主持国家“十三五”重点专项、重点项目等20余项;在Progress in Materials Science等期刊发表SCI论文200余篇;SCI他引3000余次,高被引论文15篇;授权中国发明专利14项,转让7项;作为主要研究者研发出首个国产低通和高通中空纤维膜血液透析器;获准2个III类医疗器械注册证;获国家科技进步二等奖1项,四川省优秀教学成果一等奖及二等奖各1项,宝钢优秀教师奖1项。

李育霈,四川大学2019级急诊医学在读博士研究生,导师为苏白海教授。研究生期间以第一作者或共同第一作者在Nature biomedical engineering (IF:18.952) 和 Carbohydrate polymers (IF: 7.182) 等SCI杂志发表研究论文3篇,以共同作者发表SCI论文10篇;在ASN Kidney Week 2018、ERA-EDTA 2019及中华医学会肾脏病学分会2019学术年会等国内外学术会议以第一作者发表会议论文8篇,获优秀论文奖3次;2019年10月受邀出席在日本京都举办的ISFA & JSFA 2019学术会议并作口头发言;以第二发明人申请专利2项(授权1项);获得2019年四川省“互联网+”创新创业比赛银奖、第十五届“挑战杯”四川省大学生课外学术科技作品竞赛二等奖等各类型竞赛奖项5项;以核心成员身份参与院级科研项目1项(四川大学华西医学科技成果转化基金:自抗凝壳聚糖杂合血液灌流吸附柱用于脓毒血症患者体外内毒素吸附及细菌捕获的转化研究)。

李佳梦,四川大学华西临床医学院肾脏内科2019级在读学术型博士研究生,导师为苏白海教授。
研究生期间参与国家自然科学基金1项,获得日本第一三共医药学奖学金、校级一等奖学金、 四川大学优秀研究生等荣誉。
以第一作者/共同第一作者发表SCI论文5篇。

苏白海教授团队主要研究方向为医用血液净化材料研发、急性肾损伤及慢性肾脏病-矿物质骨代谢紊乱等相关领域的临床及基础研究,拥有从事前期生物材料设计与研发、中期动物实验安全性与有效性验证及后期临床试验评价的多领域、跨学科、全方位的研究人员(其中包括1名主治医师,1名博士后及12名在读博士、硕士),现已参与并完成三个血液透析(灌流)器的转化上市。团队旨在根据临床对血液净化方式变革的迫切需求,针对不同疾病具体实际研发并转化新型血液净化材料,致力于全球领先的穿戴式人工肾的研发,以期推动全球范围内血液净化材料科研创新及成果转化再上新台阶,通过科技创新造福人类健康事业。
| 版权声明:华西微家倡导尊重和保护知识产权。欢迎转载、引用,但需取得本平台授权。如您对文章内容版权存疑,请致电028-85422587,我们会与您及时沟通处理。本站内容及图片仅供参考、学习使用,不为盈利且不作为诊断、医疗根据。 |




